如果您正在尋找相關產品或有其他任何問題,可隨時撥打公司服務熱線,或點擊下方按鈕與我們在線交流!
近年來我國雖然也在積極開發鹽湖鋰資源。但由于我國鹽湖鹵水中的鎂含量較高,鎂和鋰這兩種元素較難分離,到目前還沒有大規模的產業化生產,所以我國一直從鋰礦石中提取鋰鹽。由于不同的鋰礦物其性質差別很大,從鋰礦物中提取碳酸鋰的工藝也各不相同。
目前我國碳酸鋰生產主要以鋰云母和鋰輝石為主,鋰云母生產主要以硫酸鹽法,鋰輝石生產主要以硫酸法為主,今天給大家交流一下硫酸法生產工藝:
以鋰輝石為原料生產碳酸鋰,工業上比較成熟的工藝是硫酸法生產工藝。此工藝的基本原理在于硫酸與β-鋰輝石在250~300 ℃下發生置換反應,生成 Li2SO4。反應方程如下:
β-Li2OAl2O34SiO2 + H2SO4 -----Li2SO4 + H2O Al2O3 4SiO2。
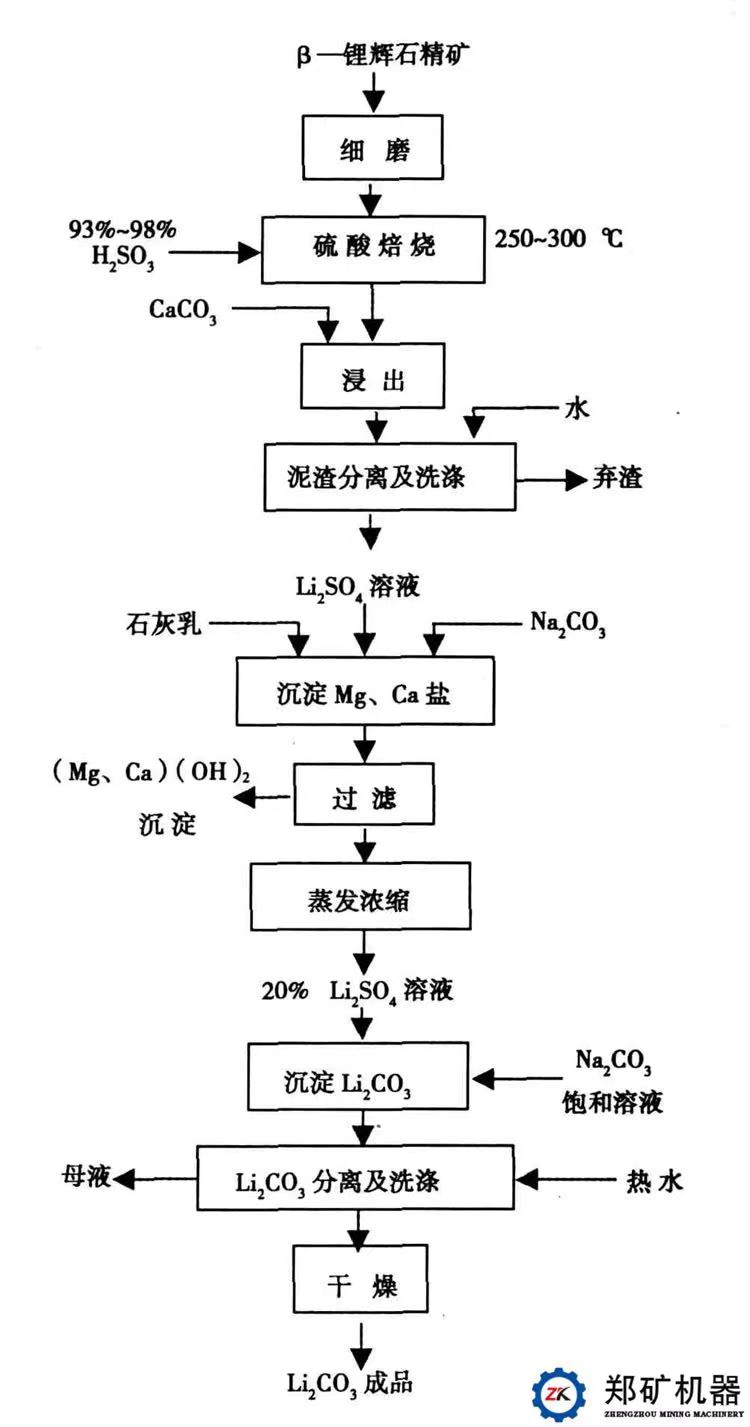
這一反應只能發生于結構較為疏松的β-鋰輝石。先將選礦獲得的含Li2O 5.5% ~7.5%的鋰輝石精礦在1050-1100℃的回轉窯中高溫焙燒,使礦石密度由 3.15g/cm3,降至2.4g/cm3生成為β-鋰輝石。冷卻后球磨至100目左右,與足量的硫酸 (93% ~98% )混合,送入250℃酸化回轉爐中進行硫酸焙燒。冷卻后水浸,加石灰石控制pH為5,得到含10%左右的Li2SO4粗鋰液,用石灰調pH至11,加碳酸鈉除鈣、鎂、鐵、鋁等雜質。清液蒸發成含12~20%左右Li2SO4的凈化液,加入碳酸鈉沉淀成碳酸鋰。離心脫水,濾渣經350℃干燥,得到碳酸鋰產品,回收率在90%左右,濾液冷卻后結晶回收硫酸鈉。
硫酸法生產碳酸鋰收率較高,并可處理Li2O含量僅110%~115%的礦石。但是相當數量的硫酸和純堿變成了價值較低的Na2SO4, 應盡可能降低硫酸的配量。此方法最大優點是浸取燒結所得的溶液中含有110~150 g/L硫酸鋰,經過浸取即可得到比較純凈的溶液。硫酸法也可用來處理鋰云母和磷鋁石。
